In Europa l’utilizzo del rame per la difesa delle colture, rientrando questa sostanza attiva nella categoria dei “candidati alla sostituzione” in base al Reg. 1107/09, è stata rinnovata per soli 7 anni fino al 31 dicembre 2025.
Oltre questo termine la sostanza attiva deve essere rivalutata. Al momento, sono autorizzati gli impieghi che comportano un’applicazione totale non superiore a 28 kg di rame per ettaro nell’arco di 7 anni. Una quantità definita al fine di evitare effetti inaccettabili sull’ambiente, ma è facoltà degli Stati Membri fissare limiti più restrittivi come quello di fissare un valore massimo di applicazione annuo non superiore a 4 kg/ha. I Sali di rame, per esempio, sono vietati sia per il biologico che per l’agricoltura convenzionale in paesi Ue come i Paesi Bassi e la Danimarca. L’Italia, invece, ha optato per il mantenimento della flessibilità concessa agli stati membri.
Articolo pubblicato sulla rubrica Primo Piano di Terra e Vita
Abbonati e accedi all’edicola digitale
Verso ulteriori restrizioni?
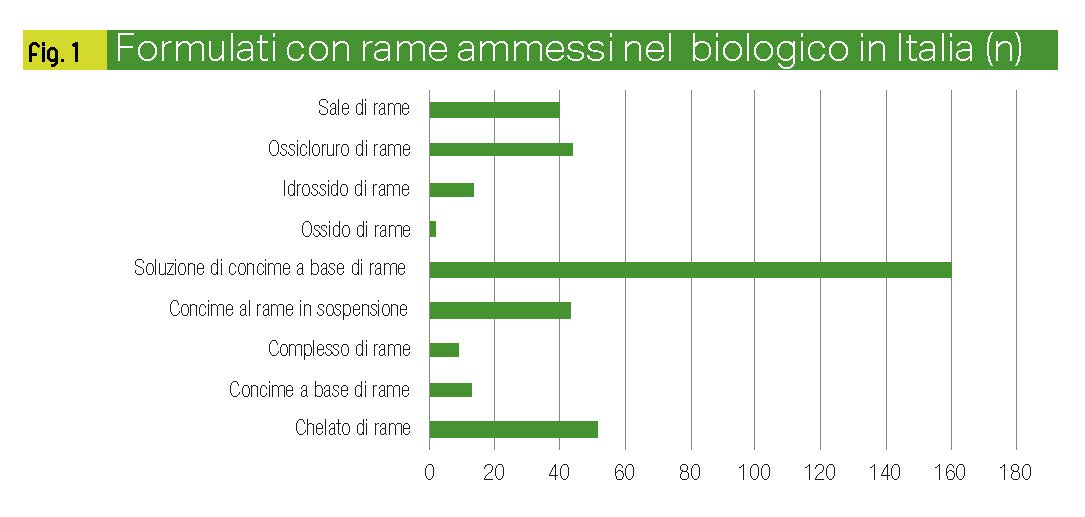
Tenendo conto della recente evoluzione della normativa relativa all’uso di questi prodotti in agricoltura biologica, ed essendo vicino il termine per la rivalutazione della sostanza attiva, si temono tuttavia ulteriori restrizioni nel prossimo futuro. Anche perchè, contro ogni previsione della normativa europea, la restrizione d’impiego dei Sali di rame ha, di fatto e innegabilmente, comportato un maggiore utilizzo di fertilizzanti fogliari contenenti questo “nutriente”, di fatto impiegato però contro i patogeni delle piante (fig. 1).
Per fare fronte a ciò In Italia, sia in ambito di produzione integrata che biologica, si è tentato di imporre di definire l’effettivo quantitativo di rame distribuito ad ettaro all’anno conteggiando tutti gli apporti di rame sulla coltura sia come prodotti fitosanitari che fertilizzanti o altri prodotti similari dove sia contenuto il sale di rame.
 Task force al lavoro
Task force al lavoro
In favore della proroga dell’autorizzazione di questo storico prodotto sta lavorando l’European Union Copper Task Force, che punta rivedere i criteri di valutazione. I criteri Pbt (ovvero persistenza, bio-accumulo e tossicità), infatti, furono sviluppati dalle autorità ambientali europee per le sostanze inquinanti organiche persistenti e non è applicabile alle sostanze inorganiche. In altre normative europee come il Reg. 528/2012 sui biocidi (Bpr) e il Reg. 1907/2006 sulla registrazione delle sostanze chimiche (Reach) il rame viene esentato da tale valutazione in quanto sostanza inorganica.
L’Efsa (European Food Safety Agency) ha pubblicato nel 2021 un documento dove conferma che nessuno dei modelli attualmente disponibili è in grado di simulare in maniera appropriata il destino ambientale delle sostanze come il rame e sottolinea la necessità di considerare alla base della valutazione i fattori di solubilità, biodisponibilità e controllo omeostatico, suggerendo l’utilizzo di modelli (suolo, acque superficiali e di falda, sedimenti) e approcci diversi da quelli standard applicabili alle sole sostanze di sintesi organica e maggiormente adatti alla valutazione dell’impatto ambientale del rame.
A livello europeo si sta peraltro assistendo ad un braccio di ferro tra chi sostiene la riatorizzazione e chi invece presuppone che i sali di rame non siano più così insostituibili nella difesa delle colture dalle malattie batteriche e fungine. È tuttavia una tesi scientificamente condivisibile?
Vediamo i punti a favore e contro. ovvero le frecce nell’arco di chi sostiene le due tesi.

Lo ione Cu nel terreno
Molti di questi problemi dipendono dal comportamento dello ione Cu, che è una forma tossica per piante e microrganismi, nel terreno. Qui si lega a particelle di materia organica, argilla e idrossidi di metalli. Il movimento dello ione verso il basso attraverso il profilo del suolo è quindi maggiore nei terreni sabbiosi rispetto ai suoli ricchi di argilla o sostanza organica. Inoltre la sua disponibilità e tossicità viene notevolmente aumentata se il pH del suolo diminuisce.
A pH più alto, infatti, lo ione Cu rimane in forma insolubile. Lo ione Cu che liscivia attraverso il profilo del terreno e i possibili effetti tossici sulle colture perenni potrebbero essere mitigati aumentando il pH del suolo e/o accumulando il contenuto di materia organica del terreno o applicando gesso per ridurre la sua tossicità nel terreno.
Il meccanismo d’azione
Il rame è un micronutriente essenziale per tutti gli organismi viventi e funge da cofattore per diversi enzimi coinvolti nella respirazione e nelle proteine di trasporto degli elettroni. Allo stesso tempo il rame, a concentrazioni più elevate, agisce come un biocida ad ampio spettro a causa della sua interazione con gli acidi nucleici, l’inibizione dei siti attivi degli enzimi, l’interferenza con il sistema di trasporto dell’energia e, infine, la rottura dell’integrità delle membrane cellulari. Diverse formulazioni di Cu inorganiche sono state sviluppate e utilizzate come biocidi per contenere batteri fitopatogeni, funghi, oomiceti e, in alcuni casi, invertebrati e alghe. Oltre all’applicazione diretta sulle piante in campo, i Sali di rame vengono utilizzati anche per il trattamento di concia delle sementi.
L’ampia disponibilità di prodotti a base di rame ne ha facilitato l’impiego su svariate colture annuali e perenni, principalmente per gestire le malattie, in particolare in agricoltura biologica. Tra le più importanti malattie delle colture gestite con prodotti rameici, troviamo quelle causate da oomiceti come, la peronospora della vite e della patata. Per il loro basso costo i Sali di rame sono importanti, anche nell’agricoltura convenzionale e hanno ampio impiego quando i fungicidi autorizzati vengono vietati a causa dei loro effetti negativi sulla salute umana e biodiversità. Questo è particolarmente vero per le colture cosiddette “minori” nei casi in cui un certo numero di prodotti fitosanitari, in passato autorizzati, non siano più disponibili.

Funghi e batteri senza alternative
In generale le malattie fogliari più controllate dai composti rameici sono: peronospora, ticchiolatura, ruggine, bolla, occhio di pavone, ma sono davvero pochi i prodotti fitosanitari in grado di proteggere le colture dalle malattie batteriche.
Di conseguenza i prodotti a base di rame sono spesso l’unico mezzo disponibile per i coltivatori sia nell’agricoltura convenzionale che biologica per gestire le malattie causate batteri fitopatogeni, come per esempio le batteriosi del pomodoro, il cancro batterico degli agrumi, il colpo di fuoco batterico delle pomacee, la batteriosi del noce, il cancro batterico delle drupacee e la rogna dell’olivo.
Le uniche eccezioni sono il colpo di fuoco batterico di pomacee e il cancro batterico del kiwi, per i quali è disponibile un discreto numero di agenti di controllo biologico che, a onore del vero, seppur validi, non sembrano al momento avere la stessa efficacia dei prodotti rameici. In più, recenti ricerche hanno messo in evidenza anche altre interessanti attività del metallo, che vanno ben oltre la semplice azione “fungicida” diretta.

Le ultime scoperte
Il rame, infatti, anche a bassissime dosi, è implicato in diversi processi di induzione di resistenza (elicitore). Lavori sperimentali effettuati su Arabidopsis, olivo, pomodoro, vite, patata ecc., relativamente ad alcuni funghi patogeni (es. peronospore) e batteri, hanno verificato che il rame induce la produzione di ROS (reactive oxygen species) e l’accumulo e deposito di callosio, oltre che l’espressione dei geni PR (proteine correlate con la patogenesi) e delle vie di segnalazione della MAP- chinasi.
I ROS possono avere azione tossica diretta sul patogeno o fungere, a loro volta, da “messaggeri” chimici di difesa. Il callosio è una sostanza polimerica di contenimento che permette di confinare i funghi nei punti di infezione; può generare papille che inglobano gli organi di nutrizione del fungo (appressori, austori) dopo l’infezione, in modo da creare una sorta di tessuto connettivo che limita il propagarsi del patogeno.
In Francia ricercatori dell’Inrae hanno trovato che su vite il rame è altresì implicato nei processi di produzione di ossilipine e quindi di jasmonati. Le ossilipine derivano per ossidazione enzimatica (lipossigenasi) o non enzimatica (auto-ossidazione mediata da ROS) degli acidi grassi polinsaturi linoleico e linoleico. Per successive reazioni possono originare acido jasmonico, molecola coinvolta nei processi di difesa contro stress biotici e abiotici delle piante. Il rame sarebbe in grado, probabilmente, di indurre la produzione di ROS e, di riflesso, l’ossidazione degli acidi grassi (ossidazione non enzimatica). Lavori effettuati su patata e pubblicati sulla rivista Molecular Plant Pathology hanno anche accertato l’attività “indiretta” del rame sulla Phytophthora infestans mediante inibizione della sintesi di ABA (il rame sopprime la trascrizione dei geni coinvolti nella sintesi dell’acido abscissico-ABA), con conseguente diminuzione del contenuto dell’ormone e stimolazione della sintesi di etilene. In alcuni patogeni la riduzione di ABA stimola la sintesi del callosio e dell’acido salicilico, molecole coinvolte, entrambe, nei processi di difesa.
Questo breve excursus mette in evidenza la complessità dell’azione del rame nella difesa fitosanitaria. Sicuramente ulteriori ricerche sono necessarie, ma è già possibile intravedere una “nuova vita” per uno degli elementi “insostituibili” nella fitoiatria moderna.

Gli aspetti negativi
L’uso intensivo dei Sali di rame per più di un secolo ha portato a una serie di impatti negativi sulla biodiversità e sulla salute umana. Mentre nel secondo caso I principali effetti negativi vengono limitati dagli stessi produttori ormai ampiamente in grado di rispettare i tempi di carenza, nel primo caso gli aspetti negativi sono legati a:
- accumulo nel terreno ed effetti negativi sul bioma del suolo;
- fitotossicità;
- sviluppo di ceppi resistenti.
Effetti sul bioma del suolo. Gli effetti negativi sono stati osservati anche per molti macro-organismi come le popolazioni di lombrichi, nematodi e lumache. Nella maggior parte dei suoli, è probabile che i residui rameici rimangano indefinitamente continuando ad influenzare la salute del suolo. Inoltre, livelli elevati di rame possono causare la contaminazione delle acque superficiali e sotterranee.
Fitotossicità. Sono svariati i fattori in grado di causare fitotossicità da Cu sulle piante, compresa l’applicazione di formulazioni di Cu altamente solubili (ad es. solfato di rame, nitrato di rame) o quantità eccessive (dose di applicazione troppo elevata o applicazioni troppo frequenti), impiego di soluzioni a pH acido (inferiore a 5,5) che si tradurrebbe in un eccesso di Cu solubile, miscelazione estemporanea di Sali di Cu nell’atomizzatore con altri prodotti non del tutto compatibil, applicazioni di Sali di Cu a temperature elevate, clima secco e presenza di impurità all’interno del prodotto commerciale. Inoltre, l’apparato vegetativo delle piante in condizioni di elevata umidità dell’ambiente, favorisce un rilascio continuo di ioni Cu con conseguenti effetti potenzialmente fitotossici. Infine, l’applicazione dei prodotti rameici in determinate fasi fenologiche della coltura potrebbe provocare altrettanti effetti fitotossici in quanto le piante in alcune fasi, come per esempio la fioritura, sono sensibili ai composti di Cu anche a concentrazioni inferiori. Tutti questi fattori sono ben conosciuti dai produttori e dai tecnici durante i moltissimi anni di impiego di questo sale, e pertanto opportunamente evitati in campo.
Articolo pubblicato sulla rubrica Primo Piano di Terra e Vita
Abbonati e accedi all’edicola digitale
Sviluppo di ceppi batterici resistenti al rame. Anche se i prodotti rameici hanno un’attività multisito che dovrebbe comportare un basso rischio di sviluppo di resistenza da parte degli agenti patogeni, in tutto il mondo sono stati segnalati dei casi in alcune specie di batteri fitopatogeni.
Negli anni a forte pressione epidemica può essere infatti necessario intervenire spesso durante la stagione vegetativa. E nel caso in cui un ceppo batterico acquisisse resistenza al rame, la continua pressione di selezione aumenterebbe gradualmente la frequenza della popolazione patogena resistente e ne comprometterebbe, nel tempo, l’efficacia. Questo è particolarmente vero su colture arboree a causa della natura epifitica e parzialmente endofitica della maggior parte dei batteri fitopatogeni che potrebbero fungere da serbatoio di geni di resistenza al rame ed essere potenzialmente acquisiti da ceppi sensibili.
Poiché molte popolazioni batteriche prosperano sullo stesso ospite, per alcuni ricercatori potrebbe esistere il rischio potenziale di trasferimento genico orizzontale dei geni determinanti la resistenza al rame. È altamente improbabile che i batteri diventino resistenti al rame attraverso mutazioni spontanee poiché la resistenza al Cu è regolata da diversi geni nei batteri. Tuttavia in natura, non può essere escluso il trasferimento cromosomico di resistenza al Cu da parte dei plasmidi, seppure in condizioni sperimentali. La questione è come si vede è ancora molto dibattuta a livello scientifico, mentre l’applicazione pratica fitoiatrica nella stragrande maggioranza dei casi non sembra rilevare casi degni di nota. Pertanto la problematica sembra essere al momento confinata a livello accademico.
Gli autori sono del Servizio Fitosanitario – Regione Emilia-Romagna















